
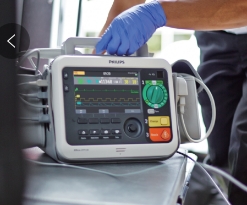
迈瑞除颤监护仪d2
上海自提或三方快递

注册证编号 国械注准20233080802 注册人名称 深圳迈瑞生物医疗电子股份有限公司 注册人住所 深圳市南山区高新技术产业园区科技南十二路迈瑞大厦1-4层 生产地址 深圳市光明新区南环大道1203号 产品名称 体外除颤监护仪 管理类别 第三类 型号规格 BeneHeart D20、BeneHeart D20C、BeneHeart D50、BeneHeart D50C 结构及组成/主要组成成分 产品由主机、电池以及附件组成,附件信息见附页。 适用范围/预期用途 BeneHeart D50/BeneHeart D50C型体外除颤监护仪用于对患者进行手动体外除颤、半自动体外除颤、起搏治疗和心电(ECG)、脉搏血氧饱和度(SpO2)、无创血压(NIBP)、有创血压(IBP)、体温(TEMP)、呼吸(RESP)、二氧化碳(CO2)监护,可以显示、回顾、存储和打印监护信息。监护参数适用于成人、小儿和新生儿。BeneHeart D20/BeneHeart D20C型体外除颤监护仪用于对患者进行手动体外除颤、半自动体外除颤、起搏治疗和心电(ECG)、脉搏血氧饱和度(SpO2)、无创血压(NIBP)、呼吸(RESP)、二氧化碳(CO2)监护,可以显示、回顾、存储和打印监护信息。监护参数适用于成人、小儿和新生儿。1.手动体外除颤功能适用于无呼吸和无脉搏的室颤以及室速患者。同步复律功能适用于终止房颤。2.半自动体外除颤功能适用于符合以下情况的心脏骤停患者:丧失反应性、无呼吸或呼吸不正常。该功能仅适用于年龄大于等于29天的患者。3.起搏功能适用于对心动过缓的患者进行治疗。如果处理及时,它同样有助于对停搏患者进行治疗。该产品支持在院前或院内使用,且只能由受过该设备操作培训并接受过基本生命支持和高级心脏支持培训的合格医务人员使用。 产品储存条件及有效期 附件 产品技术要求 其他内容 / 备注 / 审批部门 国家药品监督管理局 批准日期 2023-06-13 生效日期 有效期至 2028-06-12
对(迈瑞除颤监护仪D2)询价,索取(迈瑞除颤监护仪D2)彩页,(迈瑞除颤监护仪D2)需要维修,需要授权,请联系我们总部客服转接:400-901-5099
温馨提示:1.迈瑞除颤监护仪D2可能含有禁忌内容或者注意事项,具体详见说明书;2.购买迈瑞除颤监护仪D2后应仔细阅读迈瑞除颤监护仪D2说明书或者在医务人员的指导下购买和使用;3.以上迈瑞除颤监护仪D2内容均来自于生产厂家、代理商网站不作为宣传购买依据如与迈瑞除颤监护仪D2说明书有冲突的,均以迈瑞除颤监护仪D2说明书为准;
以下为公司资质:















 发送给微信朋友或者点击
发送给微信朋友或者点击
 分享到朋友圈
分享到朋友圈